痛み止めといえばNSAIDs!
中でも、COX-2(コックスツー)選択的阻害薬は慢性的な痛みによく使われています。セレコキシブやエトドラク、メロキシカムなどが代表ですね。
COX-2選択的阻害薬のメリットは、副作用が起こりにくいこと。胃にやさしいし、腎臓にも負担が少ない?とか……で、安全性の高さが売りです。
しかし、

・本当に、そうなのか?
・そう言い切ってよいのか?
というのが今回のテーマです。
本記事では、COX-2選択的阻害薬のピットフォールをまとめました。
大きく3つです。
- 胃障害のリスク
- 腎障害のリスク
- 心血管障害のリスク
さっそく、見ていきましょう。
NSAIDsとは
まずは基本情報を確認します。
英語では
日本語では
作用機序
非選択的NSAIDsとCOX-2選択的阻害薬
NSAIDsは大きく2種類に分けられます。
- 非選択的NSAIDs
- COX-2選択的阻害薬
COXは2種類のアイソザイムがあります。COX-1はほとんどの細胞で常時発現しており、主に生体保護・細胞の機能維持が役割です。一方で、COX-2は炎症時に誘導され、腫脹や痛みなどを引き起こします。
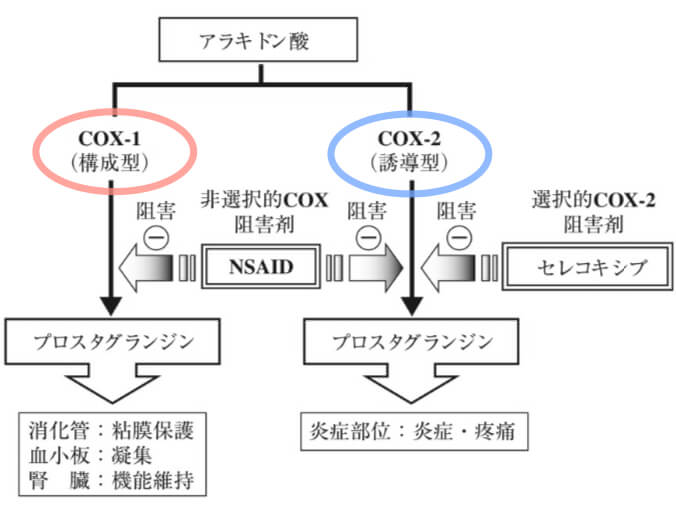

阻害活性の強さ(選択性の違い)により、非選択的NSAIDsとCOX-2選択的阻害薬に分類するのが一般的です。
国内で使用できるCOX-2選択的阻害薬は3つあります。
| 一般名 | 商品名 | 構造(分類) |
|---|---|---|
| セレコキシブ | セレコックス | コキシブ系 (COX-2阻害薬) |
| エトドラク | ハイペン | ピラノ酢酸系 (COX-2選択的阻害薬) |
| メロキシカム | モービック | オキシカム系 (COX-2選択的阻害薬) |
セレコキシブはCOX-2をターゲットに開発された世界初のコキシブ系の薬剤です。COX-2阻害薬に分類されています。一方で、エトドラクとメロキシカムはNSAIDsとして開発された後にCOX-2選択性の高さが明らかになった製剤です。選択的COX-2阻害薬と呼ばれています。


ロフェコキシブ(販売中止、後述します)がダントツですね。セレコキシブよりもエトドラクとメロキシカムの方がCOX-2の選択性が高いのは驚きでした^_^
COX-2選択的阻害薬の胃障害リスク

非選択的NSAIDsに比べて
「COX-2選択的阻害薬は胃の負担が少ない」
これはその通りです。COX-2選択的阻害薬は非選択的NSAIDsに比べて、潰瘍発症率のリスク低下が認められています。
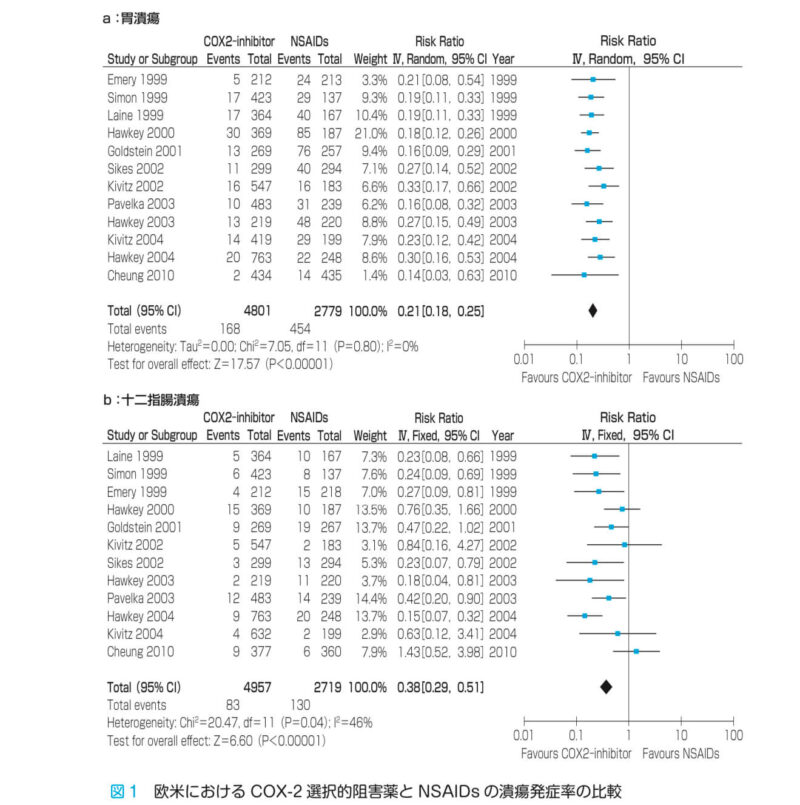
潰瘍発症率:COX-2選択的阻害薬 vs NSAIDs
欧米:COX-2選択的阻害薬とNSAIDsの潰瘍発症率の比較

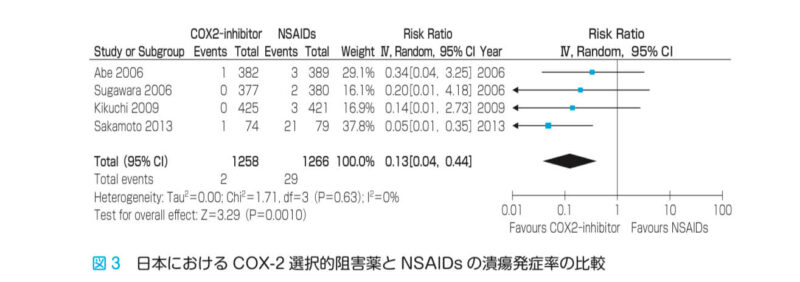
日本:COX-2選択的阻害薬とNSAIDsの潰瘍発症率の比較

COX-2選択的阻害薬が胃に優しい理由
- COX-2選択的阻害薬はなぜ胃障害のリスクが低いのか?
-
胃粘膜組織で常に発現しているCOX-1の阻害効果が弱いからです。COX-1はプロスタグランジンの産生により、粘液の分泌や胃血流量の増加など、組織の機能を維持する役割があり、COX-1阻害作用が強い非選択的NSAIDsの投与は、胃の恒常性を破綻させ、胃炎や胃潰瘍などを引き起こします。
COX-2選択的阻害薬のガイドラインでの位置付け
消化管障害のリスクを軽減するために、COX-2選択的阻害薬の投与が推奨されています。
NSAIDs潰瘍発症の予防にCOX-2選択的阻害薬の使用を推奨する
【推奨の強さ:強 エビデンスレベル:A】
これが基本の考え方ですね。実際に当院でも、安全性を考慮してCOX-2選択的阻害薬を第一選択としている医師(特に消化器内科の先生)は多いです。
一次予防の場合
COX-2選択的阻害薬は単独療法でOKです。つまり、潰瘍の既往歴がない人では、PPI等の潰瘍予防薬を併用する必要はありません。
COX-2選択的阻害薬服用時に潰瘍発生予防治療は必要か?
胃十二指腸潰瘍既往歴のない患者では潰瘍予防薬の併用は必要ないが、胃十二指腸潰瘍や潰瘍出血の既往歴がある患者ではPPIによる潰瘍発生予防治療を行うことを推奨する
【推奨の強さ:強、エビデンスレベル:B】
非選択的NSAIDsの場合は、一次予防においてもPPIの投与が提案されています。
NSAIDs潰瘍の発生予防は潰瘍既往歴がない患者においても必要であり、PPIによる予防を行うように提案する
【推奨の強さ:強、エビデンスレベル:A】
これは、保険適用外ですが…。
一方で、ハイリスク患者の場合
潰瘍既往歴のある患者のNSAIDs潰瘍の予防には、PPIを推奨し、ボノプラザンを提案する
【推奨の強さ:弱、エビデンスレベル:B】
出血性潰瘍既往歴のある患者のNSAIDs出血性潰瘍の再発予防には、COX選択的阻害薬にPPI併用を推奨する
【推奨の強さ:強、エビデンスレベル:B】
二次予防では、再燃リスクが高くPPIの併用が推奨されています。最近ではボノプラザン(Pcab)を使用するケースも多いです。さらにハイリスクである出血性潰瘍既往の患者では、非選択的NSAIDsではなく、COX-2選択的阻害薬の使用が推奨されています。潰瘍予防薬の併用だけでは足りず、NSAIDs自体をCOX-2阻害薬に変更して潰瘍リスクを極力下げるわけですね。
COX-2選択的阻害薬のピットフォール
ここまでの内容をまとめると、COX-2選択的阻害薬のメリットは非選択的NSAIDsよりも胃障害のリスクが低い点です。



じゃあ、消化管障害のリスクを考慮して、とりあえずCOX-2阻害薬を処方しておけば安心なのか?
というと、そうではなくて、COX-2阻害薬にも落とし穴があります。COX-2は炎症時に誘導され、傷ついた粘膜を修復する働き(COX-1の代償)もあるからです。不快な痛みや腫れを起こすのでいつも悪者扱いされがち……ですが、実は生体にとって大事な役割もあります。
NSAIDs潰瘍は2つの要因で起こるという理解です。
- COX-1阻害による粘膜障害
- COX-2阻害による組織治癒の遅延(代償作用の妨げ)
COX-1だけで粘膜障害が起こるわけではありません。傷ついた組織を修復するためにCOX-2の代償作用が働くからです。両方の阻害により、生体の恒常性が破綻すると考えられています。
COX-2選択的阻害薬は、COX-1に対する影響が弱く、組織へのダメージは与えにくいけど、傷ついた組織の回復を遅らせてしまう可能性があります。ここが弱点です。
だから、COX-2選択的阻害薬といえども、ノーリスクではありません。実際に低用量アスピリン(LDA)との併用で潰瘍リスクの増加が認められます。
消化管出血リスク
| Cases | Control | Age adjusted RR (95%CI) | Adjusted condition RR (95% CI)* | |
|---|---|---|---|---|
| Non-use | 2356 | 5020 | Reference | Reference |
| Coxib only | 28 | 63 | 1.0 (0.6 to 1.5) | 1.0 (0.5 to 1.8) |
| Low‐dose aspirin only | 366 | 379 | 2.3 (2.0 to 2.7) | 3.6 (2.9 to 4.5) |
| Coxib and low‐dose aspirin | 6 | 4 | 3.7 (1.0 to 13.1) | 14.5 (3.3 to 63.9) |
*Adjusted for age, sex, calendar semester, ulcer history, nitrates, anticoagulants, antiplatelets and acid‐suppressing drugs.
†Categorised only among NSAID current single users.
単独療法ではリスクが低いCOX-2阻害薬であっても、併用によってメリットが失われるわけです。一般的な感覚では、消化管障害リスクが低いとされるCOX-2阻害薬にも、組織の治癒を妨げるというピットフォールがあります。
LDAにセレコキシブを併用する場合には、潰瘍リスクに備え、単独療法ではなくPPIの予防投与が必要です。もちろん、一次予防では保険適応外になります。
LDAとNSAIDs併用による潰瘍再発予防にはLDAとセレコキシブにPPIの併用を推奨する
【推奨の強さ:強、エビデンスレベル:A】


COX-2選択的阻害薬の腎障害リスク

非選択的NSAIDsに比べて
「COX-2選択的阻害薬は腎臓の負担が少ない」
答えはNOです。腎障害のリスクはどちらも変わりません。
COX-2選択的阻害薬と非選択的NSAIDsはどちらも、腎障害を引き起こす可能性があります。
COX-2選択阻害薬とCOX-2非選択薬は同等に急性腎障害を発症させるため、COX-2選択性に限らず NSAIDsの使用の際には虚血性腎障害の発症に注意する必要がある
【推奨の強さ:弱い、エビデンスレベル:強い】
NSAIDsで腎障害が起こる理由
- なぜ、NSAIDsは腎障害を引き起こすのか?
-
NSAIDsはプロスタグランジン(PG)の合成阻害により、糸球体の輸入細動脈を収縮し、糸球体内圧減少による糸球体ろ過量(GFR)の低下を招くからです。PGは腎血流量を調節する役割があります。
COX-2選択的阻害薬のピットフォール



腎機能が良くないしCOX-2阻害薬にしとこうかなぁー
ときどき耳にする言葉ですよね?!NSAIDsは腎臓に負担がかかるのはよく知られた事実。けれども「安全性が高いCOX-2阻害薬であれば大丈夫」と、考えてしまう傾向があるように思います。



でも、COX-2阻害薬は腎障害のリスクが低いわけではありません。
なぜなら、胃粘膜組織と違って腎臓では恒常的にCOX-2が発現しているからです。ここを誤解されてる人、意外と多くて私もCOX-2選択的阻害薬の方が安全だと思ってました。でも、そうではなくてCOX-2阻害薬を選んでも、腎障害のリスクを軽減させることはできません。
eGFR30未満は禁忌!
COX-2選択的阻害薬と非選択的NSAIDsはどちらも、重篤な腎機能障害のある方に投与できません。腎機能を悪化させる可能性があるからです。eGFR30-59の方は慎重投与で、短期間の使用に留める必要があります。
30mL/min未満:腎障害を悪化させるおそれがあるため、重篤な腎障害には禁忌
30-59mL/min:高齢者、高血圧患者、糖尿病患者、心不全患者、利尿薬の併用されている症例など腎障害のリスクの高い患者には漫然と投与しないこと
電子添文の表記
| セレコックス | モービック | ハイペン | |
|---|---|---|---|
| 重度腎機能障害 | 禁忌 | 禁忌 | 禁忌 |
| 腎機能障害又はその既往歴のある患者 | 慎重投与 | 慎重投与 | 慎重投与 |
「腎機能が良くないしCOX-2阻害薬にしとこうかなぁ?」という誤解に遭遇したら「非選択的NSAIDsとCOX-2阻害薬、どちらも腎障害のリスクは変わらないので、アセトアミノフェンなどへの変更は可能でしょうか?」と、処方提案を進めて誤解を解く必要があります。


COX-2選択的阻害薬の心血管リスク


非選択的NSAIDsに比べて
「COX-2阻害薬は心血管イベントのリスクを増加させる」
という報告があります。
これは意外と知らない人が多いかも知れません(私は記事を書くにあたって知りました^ – ^)
COX-2阻害薬ロフェコキシブ(国内未承認)は心血管イベントリスク増加の報告を受けて、販売中止に追い込まれました。パレコキシブとバルデコキシブも同リスクに加え、重篤な皮膚障害を理由に市場から撤退しています。
- 2000年、VIGOR試験(リウマチ患者)の後解析
-
ロフェコキシブはナプロキセンに比べて、心血管イベントが2.38倍に増加
- APPROVe試験(大腸ポリープ再発予防)
-
ロフェコキシブはプラセボに比べて、心血管イベントが1.92倍に増加
- 2005年、CABG後の疼痛コントロール試験
-
パレコキシブ(プロドラッグ、注射)に続く、バルデコキシブ(経口)はプラセボに比べて、心血管イベントを約3.7倍に増加



では、国内発売のセレコキシブは心血管障害のリスク、大丈夫なのか?
- 2005年のAPC試験(大腸ポリープ再発予防)
-
セレコキシブはプラセボに比べて、心血管系事象のリスクが400mg/日群で2.3倍、800mg/日群3.4倍に増加
用量依存的なリスク上昇が判明、試験は中止になりました
- その後のpreSAP試験(大腸ポリープ再発予防)
-
セレコキシブはプラセボに比べて、心血管リスクが400mg×1/日で有意差なしという結果でした
セレコックスは心血管リスクに累積性が認められず、ロフェコキシブなどのように販売中止を免れました。
- PRECISION試験
-
セレコキシブの安全性は、非選択的NSAIDsに劣らないことが示されました
・対象者…心血管リスクがあり、慢性関節炎で疼痛管理が必要な患者24,081名
・一次エンドポイント…心血管死、非致死的心筋梗塞、脳卒中の発生率・結果は以下のとおり
・セレコキシブ群で2.3%(209mg/平均1日用量)
・ナプロキセン群で2.5%(852mg/平均1日用量)
・イブプロフェン群で2.7%(2045mg/平均1日用量)
最終的には、セレコキシブの心血管リスクは他のNSAIDsと比べて変わらないとの結論です。ただし。添付文書の警告には以下の記載があり、注意喚起がされています。
(警告)外国において、シクロオキシゲナーゼ(COX)-2選択的阻害剤等の投与により、心筋梗塞、脳卒中等の重篤で場合によっては致命的な心血管系血栓塞栓性事象のリスクを増大させる可能性があり、これらのリスクは使用期間とともに増大する可能性があると報告されている
(禁忌)冠動脈バイパス再建術の周術期患者[外国において、類薬で心筋梗塞及び脳卒中の発現が増加するとの報告がある
セレコックス錠 電子添文
COX-2阻害薬がイベントリスクを増加させる理由
- どうして、COX-2阻害薬は心血管イベントを増加させるのか?
-
プロスタグランジンPGI2産生低下(血管のCOX-2阻害)と相対的なトロンボキサンTXA2増加(血小板にはCOX-2なし)により、血管収縮と血小板凝集が優位になるためと考えられています(FitzGeraldの仮説)。

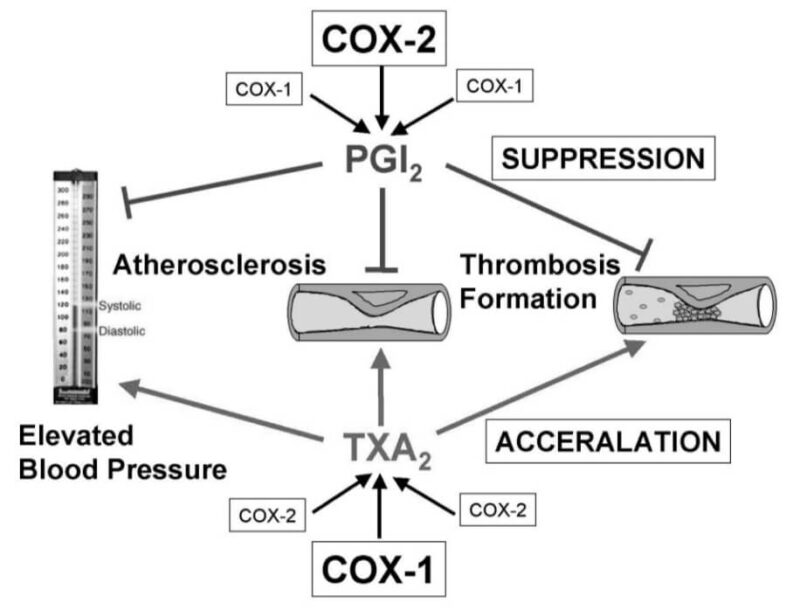
Inflammation and Regeneration Vol.25 No.6 NOVEMBER2005 相対的なPGI2<TXA2によって、心血管障害を引き起こすという仮説です。ちょうど、低用量アスピリンとは逆の作用ともいえますね。
NSAIDs全般で心血管リスクが増加する?!



結局のところ、COX-2選択的阻害薬の心血管障害リスクはどうなのか?
FDAは「低用量アスピリンを除くCOX-2阻害薬を含む全てのNSAIDsは心血管リスクを増加させる危険性がある」として米国では添付文書に警告を記載しています。非選択性NSAIDsでも心血管イベントを増加させるとの報告もされているからです。
ADAPT試験
約2400人の被験者を対象に、非ステロイド性抗炎症薬(NSAIDs)のアルツハイマー病予防効果を検証した試験です。
セレコキシブはプラセボと比べ、有意なリスク増加認めず。一方、ナプロキセンは心血管イベントのリスクを1.57倍に増加させました。
この結果から、一概にCOX-2選択性だけをもって心血管イベントリスクを説明するのが難しい状況になりました。
まとめると、
COX-2阻害薬を含むNSAIDs(アスピリン以外)は、投与の際に心血管リスクを念頭におく必要があると考えられます。国内の添付文書(セレコキシブを除く)では、米国のように心血管障害のリスクに関する注意喚起は見当たりませんが、特に、心血管イベントリスクの既往がある人では投与の可否を慎重に検討することが大切だといえます。
まとめ


今回はCOX-2選択的阻害薬をテーマに3つのピットフォールをまとめました。
本記事のポイント
- 胃障害リスク
-
- COX-2選択的阻害薬は潰瘍を引き起こすリスクが低い
- NSAIDs潰瘍は”COX-1阻害による粘膜障害”と”COX-2阻害による組織治癒遅延”、2つの要因で起こるという理解
- COX-2選択的阻害薬はノーリスクではない(特にLDAとの併用に注意)
- 腎障害リスク
-
- COX-2選択的阻害薬は腎臓に負担がかかりにくい?(誤解)
- COX-2は腎臓で恒常的に発現しているから
- COX-2選択的阻害薬は非選択的NSAIDsと同様にリスクがある
- 心血管リスク
-
- COX-2阻害薬は心血管イベントリスクの増加が報告されている
- PGI2産生低下と相対的なトロンボキサンTXA2増加により、血管収縮と血小板凝集が起こる(FitzGeraldの仮説が有力)
- FDAはCOX-2阻害薬に限らず、アスピリンを除くNSAIDs全般でリスクが増えるとしている
COX-2阻害薬は副作用のリスクを軽減するために開発された経緯もあって、一般的には「非選択的NSAIDsよりも安全性が高い」と思われています。しかし、使う場面や患者さんの状態によっては「COX-2選択的阻害薬を選んでおけば大丈夫」というわけではないということです。
「非選択的NSAIDsとCOX-2選択的阻害薬どちらがよいか?」日常業務で立ち止まって考える機会、ときどきあります。そんな時に、目の前の患者さんにとって妥当な方を選択できるように知識を整理しておきたいですね。

